18世紀にエドワード・ジェンナーが天然痘ワクチンを考案して以来、免疫学には長い歴史があります。長い歴史を経ても、免疫反応の仕組みについては未だ不明な部分が多々あります。 今回紹介する研究成果は、「免疫反応はどのようにして起こるのか?」という問いへの最も先進的な回答となります。生体防御を担う免疫の仕組みがより高度に解明されることによって、アレルギー治療の可能性もさらに広がっていくでしょう。

アレルギー発症の本当の仕組み 免疫反応の“はじまり”を解き明かす
アレルギーは免疫の過剰反応
アトピー性皮膚炎の悪化要因の一つに、アレルギー体質と免疫の問題があります。アレルギー症状としての皮膚炎やかゆみなどは、体の免疫反応が過剰に働くことによって起こります。本来の免疫反応は、細菌やウイルスなどの危険な異物を排除して体を守るためのもの。ところがアレルギー体質の場合は、ダニや花粉、食物など危険とはいえない異物にまで過剰反応してしまいます。
今回ご紹介する研究論文『免疫を活性化させるミクロシナプス構造を発見』は、これらの免疫反応の根本的な仕組みを解明する研究で、いかにして免疫反応が起こるのかという核心部分に迫るものです。主役となるのは、アレルギー疾患に大きな影響力を持つT細胞(免疫細胞)。本題に入る前に、T細胞の基礎知識やアトピーとの関係についてお話ししましょう。
まずは免疫反応の基本から
免疫とは、外部の侵入物から体を守るために備わった仕組みです。例えば、風邪をひくと鼻水やくしゃみ、発熱といった症状が現れます。これらの症状は、風邪ウイルスという侵入物を追い出したり殺したりするために起こる免疫反応によるものです。ダニや花粉などの異物に反応するアレルギー症状も、免疫系がそれらの異物を敵と認識することで起こる免疫反応です。
免疫が働く目的は、体を外部の敵から守ること。そのためには、敵を見分けてやっつけなければなりません。T細胞、B細胞、樹状細胞、マスト細胞、マクロファージなどの免疫細胞は、連携してそれぞれの役割を果たすことで外敵を撃退します。その流れを簡単に説明すると、上の〈免疫反応の流れ〉のようになります。
免疫反応の流れ
- 敵を発見する
樹状細胞やマクロファージが細菌やウイルス、アレルゲンなどの異物を見つけて食べる。 - 敵の存在を報告する
異物を食べた樹状細胞は、リンパ節に移動してナイーブT細胞に異物の情報を伝える。 - 活性化する
情報を得たナイーブT細胞は活性化されて、ヘルパーT細胞やキラーT細胞に分化・増殖する。 - 撃退指令を出す
ヘルパーT細胞は、攻撃担当細胞(キラーT細胞、B細胞など)に敵をやっつける指令を出す。 - 敵を撃退する
指令を受けた攻撃担当細胞は、それぞれの方法で敵をやっつける。キラーT細胞は敵に接着しパーフォリンという分解酵素をふりかけて殺し、B細胞は抗体を作って敵に投げつけて捕まえる。


アトピーと切っても切れない関係にあるのが免疫反応です。

最近「免疫を活性化させるミクロシナプス構造を発見」という論文がでました。

免疫反応を活性化する流れが深く解明されれば、アトピー性皮膚炎改善にも新しい治療法などが発見されそうですね。
T細胞は免疫機能の要
T細胞に着眼して〈免疫反応の流れ〉をみると、ヘルパーT細胞とキラーT細胞という2種類の細胞が活躍しています。これらの細胞は違った役割を担っていますが、もともとはナイーブT細胞と呼ばれる同じT細胞でした。ナイーブとは純真、素朴といった意味で、まだ機能を持っていないT細胞をナイーブT細胞といいます。
T細胞には様々な種類がありますが、もとをただせばナイーブT細胞となります(例外もあります)。では、機能を持たないナイーブT細胞はいつ機能を持ったT細胞に変化するのでしょうか? それはT細胞が異物(抗原)に出会ったとき。つまり、樹状細胞などが異物の情報を伝えたときに(抗原提示)、ナイーブT細胞は機能を持ったヘルパーT細胞やキラーT細胞などに分化・増殖します。
ナイーブT細胞は、樹状細胞などによる抗原提示を受けない限り活性化することはありません。活性化しないということは、機能を持ったT細胞に分化しないということ。つまり、ナイーブT細胞のままでは免疫細胞として働きません。T細胞の分化が行われなければ、免疫機能全体が損なわれることになります。「免疫機能の要(かなめ)」といわれるほど、T細胞は重要な免疫細胞なのです。
これからご紹介する『免疫を活性化させるミクロシナプス構造を発見』は、樹状細胞から抗原提示を受けたナイーブT細胞が活性化する仕組みを解明する研究です。免疫の仕組みの中でも特に重要な部分が明らかにされたのです。いよいよ本題に入りましょう。
アトピーと免疫反応

免疫反応の司令塔と呼ばれるヘルパーT細胞は、1型ヘルパーT細胞(Th1)や2型ヘルパーT細胞(Th2)などに細分化されます。情報を伝える免疫細胞(樹状細胞など)が、ウイルスや細菌の情報を伝えた場合は1型ヘルパーT細胞(Th1)、ダニや花粉などの抗原(アレルゲン)の情報を伝えた場合は2型ヘルパーT細胞(Th2)に分化します。アレルギー体質は、1型ヘルパーT細胞と2型ヘルパーT細胞のバランスで決まります。ダニや花粉などの抗原の情報が伝えられる2型ヘルパーT細胞の比率が高いとアレルギー体質になりやすいことがわかっています。
樹状細胞化からアレルゲンの情報を受け取った2型ヘルパーT細胞は、B細胞にIgE抗体を作るように命令し、大量のIgE抗体が作り出されます。
IgE抗体は、体に侵入してきたアレルゲンと結合してアレルギー反応を引き起こします。アレルギー体質の検査では必ず血液中のIgE抗体量を測定しますが、IgE抗体こそがアレルギー反応の原因だからです。
炎症やかゆみなどのアレルギー症状は、このIgEと抗原がマスト細胞(肥満細胞)に結合することでマスト細胞を活性化し、炎症やかゆみなどの原因物質となるヒスタミンやロイコトリエンなどを放出することによって起こります。
T細胞は免疫シナプスで活性化する?
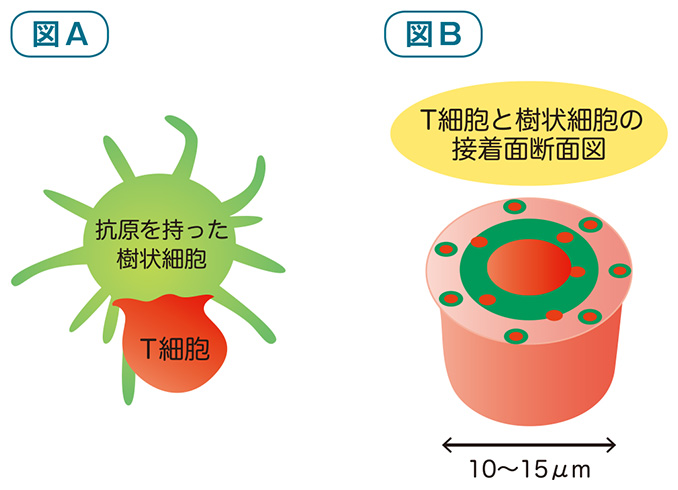
樹状細胞がナイーブT細胞に異物(抗原)の情報を伝える際、両者は図Aのようにくっつきます。このとき、樹状細胞は自分が食べた異物が外敵であるという信号を細胞表面に示します。ナイーブT細胞にはこの信号を受け取るしくみ(=抗原受容体)が備わっていて、異物が外敵であると認識します。
もう少し詳しく見てみましょう。図Bは、T細胞と樹状細胞の接着面の断面図です。図Aの二つの細胞のつなぎ目をCTスキャンのように輪切りにした様子と考えてください。
この接着面にはお互いの細胞表面受容体や細胞内の情報伝達分子が集まっていますが、その中心にはT細胞抗原受容体(赤色)が集まっており、その周りを接着分子(緑色)が取り囲んでいます。この構造を「免疫シナプス」といいます。免疫シナプスが発見されたのは今から十数年前のこと。その頃は、免疫シナプスの中心部分(T細胞抗原受容体の集まり)こそが、T細胞の抗原認識と活性化の場ではないかと考えられていました。
しかしながら、免疫シナプスがT細胞活性化の中心であると言い切るには、説明がつかない現象も確認されていました。
樹状細胞とT細胞がくっついてから免疫シナプスが形成されるまでには10~ 15 分かかるのですが、T細胞の活性化はわずか1~2分で開始されます。免疫シナプスが完成するずいぶん前から活性化が始まるという事実は、T細胞の活性化には免疫シナプス以外の要因が関係している可能性を示唆していました。

免疫反応の基本はT細胞ですが、そのT細胞が活性化する仕組みを解明したのが「免疫を活性化させるミクロシナプス構造を発見」です。

1型ヘルパーT細胞や2型ヘルパーT細胞のバランスがアトピー性皮膚炎に関係しているようですね。

そのT細胞です。T細胞は樹状細胞から抗原情報を受け取ると活性化します。この二つの細胞がくっついた構造を免疫シナプスといいます。その免疫シナプスの研究を進めてミクロクラスターが発見されたのです。
免疫反応はミクロクラスターから始まる
斉藤隆先生らの研究チームは、免疫シナプスとT細胞活性化についてさらに研究を進め、2005年に「ミクロクラスター」を発見しました。
ミクロクラスターとは、樹状細胞とT細胞がくっついた直後から現れる抗原受容体と活性化分子の複合ユニットです。
図Cをご覧ください。ミクロクラスターは免疫シナプスよりもずっと小さなものですが、理化学研究所で共同開発された生体分子イメージング(生体内の分子を可視化するシステム)という技術により、より精度の高い顕微鏡で発見されました。
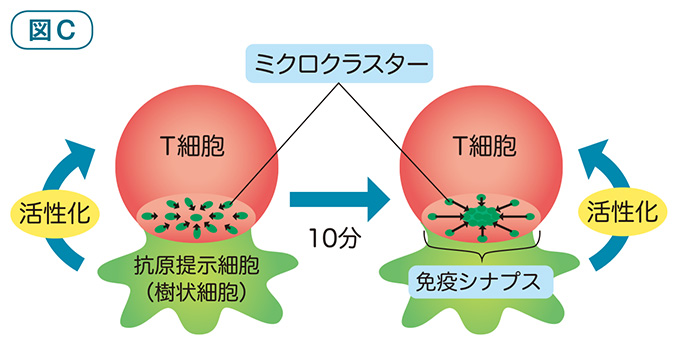
左側の図は、樹状細胞(下)とT細胞(上)が接着した直後の状態です。細胞接着面には直ちにミクロクラスターが形成され、そこからT細胞が活性化され始めます。
それから10 分後、ミクロクラスターは徐々に中心部に集まっていき、免疫シナプスが形成されるのです。免疫シナプスが形成されても、その周りではミクロクラスターが作られてT細胞の活性化が続き、免疫シナプスは1時間近く維持されます。
この研究で明らかにされたことをまとめると、
- T細胞が抗原を認識し活性化する場は、免疫シナプスではなくミクロクラスターである。
- ミクロクラスターこそが免疫応答の開始点であり、その後T細胞が活性化し続ける場所もミクロクラスターである。
ということになります。すべての免疫反応は、T細胞が活性化する場であるミクロクラスターから始めます。
ミクロシナプス構造が免疫を活性化させる
2016年に発表された『免疫を活性化させるミクロシナプス構造を発見』は、ミクロクラスターの研究をさらに進化させたものです。
免疫シナプスの形(図B)をもう一度見てください。中心に集まったT細胞抗原受容体をとり囲む緑色の部分は接着分子であると説明しました。接着分子とは、細胞と細胞をつなぐ接着剤のようなものです。
T細胞にはLFA1と呼ばれる接着分子があり、樹状細胞側の結合分子と結合することで両者はくっつきます。LFA1による接着を妨げるとT細胞は活性化しないので、接着分子がT細胞活性化に重要なことは以前から知られていました。しかし、その役割についてはよくわかっていませんでした。
研究チームは、接着分子の役割を明らかにするために、T細胞が抗原を認識した瞬間の接着分子の様子を詳細に調べました。そこで明らかとなったことを、図Dに示します。
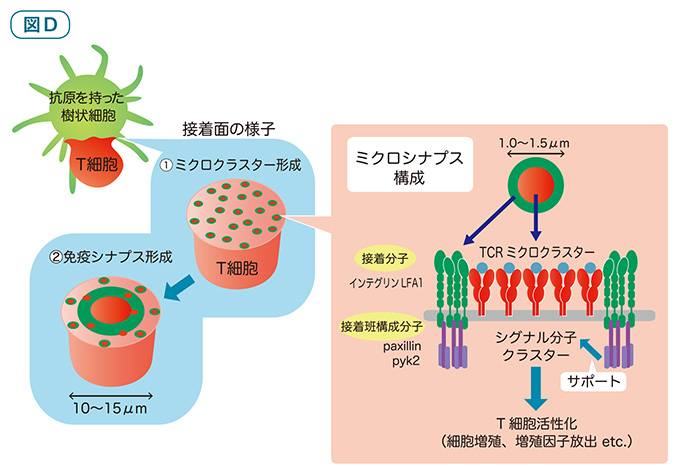
図Dの左側については、これまでの説明で理解できると思います。樹状細胞とT細胞の接着面では、接着後すぐにミクロクラスターが点々と形成され始めます(①)。10分ほどでミクロクラスターは中心に集まってきて、免疫シナプスが作られます(②)。
ここで、図中の①(ミクロクラスター形成)をよく見てください。点々と存在するミクロクラスターは、中心部が赤色でその周りを緑色が取り囲むという免疫シナプスとそっくりな形で描かれています。その拡大図が右側のミクロシナプスです。ミクロシナプスとは、今回の研究で新たに発見された細胞接着面の構造です。中央の赤色部分には、ミクロクラスターが集まっています。そして周囲を緑色の接着分子がとり囲んでいますが、接着分子の下は接着班(細胞同士が強固に接着している部分)を構成する分子がつながり、接着分子リングが形成されています。
接着分子リングは、T細胞と抗原による刺激が強いほど早く消え、結びつきが弱いとずっと続くことがわかりました。つまり、T細胞の活性化の刺激の強度によって接着分子リングが続く長さが変わるわけです。
抗原が強力であればT細胞と樹状細胞の接着時間が短くても活性化しやすく、抗原が微力な場合は接着時間を長くしないと活性化しにくくなります。接着分子リングは、抗原の強さによって接着度を変え、T細胞の活性化を調整していたのです。
最後に、斉藤先生たちの一連の研究の要点をまとめてみましょう。
- 免疫反応の出発点は、ミクロクラスターにおけるT細胞活性化にある。
- ミクロクラスターは、接着分子に囲まれたミクロシナプス構造となっている。
- ミクロシナプスでは、接着分子リングによってT細胞活性化の調整をしている。
これらの発見は、免疫の仕組みの根幹に関わる事項です。とてもベーシックな研究なので、臨床分野で応用するにはさらなる検証が必要となるでしょう。 ミクロシナプスの発見により、将来的には、接着分子リングを調節してT細胞活性化をコントロールするという新たな分子標的や治療法などが期待されます。免疫は人の健康を左右する重要な仕組みだから、この研究の応用範囲はとても広いといえるでしょう。

そのミクロクラスターという物質が免疫反応に重要な役割を果たすのですね。

ミクロクラスターがT細胞を活性化させることが解明されました。これを治療にどう活かしていくかはまだまだ時間がかかりそうですが、応用範囲は広そうです。



















コメントを残す